Souhrn
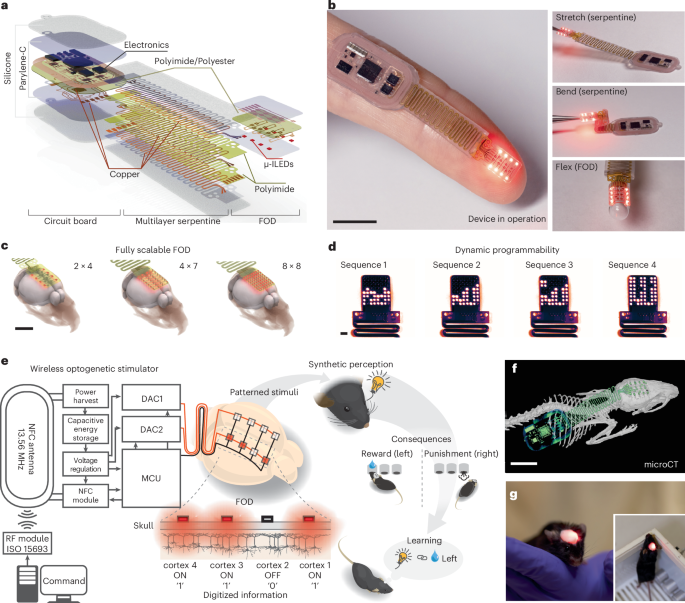
Výzkumníci vyvinuli miniaturní, plně implantabilní bezdrátové zařízení pro transkraniální optogenetickou stimulaci, které umožňuje v reálném čase patternovat aktivitu velkých kortikálních souborů u myší skrz lebku. Toto zařízení generuje umělé percepcie, které myši vnímají a dokážou je diskriminovat v chování, jako je operantní učení s odměnami. Studie kombinuje numerické simulace šíření světla a tepla s in vivo elektrofysiologií a molekulárními metodami pro validaci účinnosti.
Klíčové body
- Plně implantabilní bezdrátový stimulátor pro optogenetickou aktivaci neuronů skrz lebku bez nutnosti otevření.
- Prostorově-časové patternování stimulace velkých kortikálních oblastí v reálném čase.
- Myši úspěšně diskriminovaly umělé podněty na základě prostorové vzdálenosti mezi stimulovanými oblastmi a sekvenčního pořadí.
- Validace numerickými simulacemi pro světlo a teplo, doplněná elektrofysiologií a molekulárními analýzami.
- Potenciál pro pokročilé brain-machine interfaces s optickou komunikací.
Podrobnosti
Optogenetika je technika, při níž se do neuronů geneticky zavádějí světlem aktivovatelné iontové kanály, jako channelrhodopsin, umožňující přesnou kontrolu neuronální aktivity modrým světlem. Tradiční optogenetické metody vyžadují optická vlákna implantovaná přímo do mozku, což omezuje dlouhodobou stabilitu a invazivitu. Toto nové zařízení řeší tyto limity: je miniaturní (velikost srovnatelná s malými LED diodami), plně implantabilní pod kůží hlavy a funguje bezdrátově přes rádiové signály, které řídí patternování stimulace.
Numerické simulace modelovaly šíření světla skrz lebku a tkáně, včetně rozptylu a absorpce, stejně jako tepelné efekty, aby se zajistila bezpečnost a účinnost. Experimenty na myších s geneticky upravenými neurony pro optogenetiku prokázaly, že stimulace aktivuje velké kortikální ensembly na vzdálenosti až několik milimetrů skrz kost. In vivo elektrofysiologie měřila neuronální odpovědi, zatímco molekulární metody potvrdily specificitu aktivace.
Klíčovým testem byla diskriminace podnětů v operantním učení: myši trénované na tlakové páky musely rozlišit různé patterny stimulace (např. aktivace levé vs. pravé kortikální oblasti nebo sekvenční pořadí). Výkon myší koreloval s prostorovou vzdáleností mezi stimulovanými oblastmi – větší vzdálenost usnadňovala diskriminaci – a analýzou sekvenčního pořadí. Tato chování simulují, jak by umělé signály mohly nahradit přirozené smyslové vstupy, například v brain-computer interfaces (BCI).
Zařízení dosahuje dlouhodobé stability měsíce díky hermetickému balení a nízké spotřebě energie, což je klíčové pro chronické implantáty. Oproti elektrickým stimulacím, jako u Neuralinku, nabízí optogenetika vyšší prostorovou selektivitu (na úrovni jednotlivých neuronů) a časovou přesnost (mikrosekundy), ale vyžaduje genetickou modifikaci, což zatím omezuje na zvířecí modely.
Proč je to důležité
Tento pokrok posouvá brain-computer interfaces směrem k neinvazivnějším, optickým systémům schopným generovat komplexní umělé vnímání, což je základ pro bidirekcionální komunikaci mozku s stroji. V kontextu Neuralinku nebo jiných BCI umožňuje lepší simulaci smyslových vjemů, jako zrak nebo hmat, pro paralyzované pacienty. Pro průmysl znamená cestu k miniaturizaci a bezdrátovosti, s potenciálem pro klinické aplikace po překonání genetické bariéry (např. chemogenetikou). V širším ekosystému neurotechnologií rozšiřuje možnosti all-optical komunikace, kde vstupní signály do mozku i výstupní (např. EEG) by mohly být optické, což snižuje šum a zvyšuje přesnost oproti elektrickým metodám. Zatím je to na myších, ale validace chování ukazuje reálný pokrok k lidským aplikacím, kde by mohlo řešit slepotu nebo ztrátu končetin.
Zdroj: 📰 Nature.com